Corso di chimica generale ed inorganica 15 - gli orbitali molecolari Finora abbiamo considerato il legame come
formato dalla sovrapposizione di orbitali atomici
OA, con i loro elettroni: ogni coppia condivisa costituisce un legame. Potremmo usare anche un altro modello,
per esempio pensare ad orbitali molecolari OM e ad essi assegnare gli
elettroni di valenza. Il metodo degli OM è in effetti
più adeguato al reale. Anche per gli OM si definiscono delle funzioni d'onda Y
Ogni Y avrà, come y, dei numeri quantici, legati alla forma e all'energia E dell'orbitale; potremo così individuare orbitali molecolari s, p, d ... (in analogia con i nomi degli OA, che avevamo chiamato s, p, d, f...). Il metodo di assegnazione degli elettroni è analogo a quello dell'aufbau usato per gli OA.
La funzione Y2dt misura la probabilità di trovare l'elettrone nell'elemento di volume dt (y2dt la misura nel caso degli OA). Anche Y come y, è ottenibile per risoluzione dell'equazione d'onda di Schrödinger, in modo più o meno approssimato, date le difficoltà di risoluzione rigorosa.
Una prima approssimazione di calcolo è quella che si chiama L.C.A.O. (Linear Combination of Atomic Orbitals): le varie Y sono perciò considerate come combinazioni lineari delle y degli OA.
Se abbiamo due funzioni d'onda yA e yB per i due atomi A e B, potremo allora avere:
OM leganti (bonding) Yb= yA+ yB
OM antileganti (antibonding) Ya= yA- yB
Il numero di OM è eguale al numero complessivo di OA di valenza.
| Fig.15.1
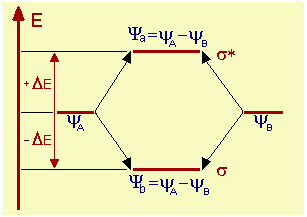
Schema energetico di formazione degli OM legante ed antilegante per la molecola H2.
La differenza di energia DE dell'orbitale legante s rispetto alla situazione degli OA è eguale, ma di segno contrario, rispetto a quella dell'orbitale antilegante s*. Perciò l'energia totale non cambia. Lo stesso schema (ma con valori di E diversi) vale anche per una ipotetica molecola di He, dato che gli OA in gioco sono gli stessi. Abbiamo a disposizione 2 OA 1s; per combinazione lineare (somma o differenza degli OA) avremo i 2 OM legante s e antilegante s*. |
 |
Nel caso della molecola di idrogeno H2, avendo due elettroni, per la regola di Pauli questi andranno nel Yb, legante s, a E più bassa di -DE rispetto alla situazione di non legame: si forma perciò un legame.
Se ci fossero altri 2 elettroni, dovrebbero andare nel Ya, antilegante, s*; questi annullerebbero l'effetto precedente di stabilizzazione del Yb: in questo caso il legame non si formerebbe poiché non ci sarebbe nessun guadagno energetico rispetto alla situazione iniziale degli OA, yA e yB.
Per He2 infatti non esiste legame, dato che dobbiamo collocare 4 elettroni.
Esiste invece He2+, s2 s*1 (2 elettroni nel legante e 1 nell'antilegante): perciò l'ordine di legame è 0,5
Usiamo il simbolo s in analogia al nome degli OA s, e così pure p in analogia ai p, e d in analogia ai d. Anche questi OM, come gli OA, hanno specifiche caratteristiche di simmetria:
OA |
OM |
caratteristiche di simmetria rispetto all'asse di legame |
s |
s |
simmetria assiale; coassiale con l'asse di legame |
p |
p |
piano nodale contenente l'asse di legame |
d |
d |
due piani nodali perpendicolari intersecantesi lungo l'asse di legame |
Fig.15.2 Corrispondenza degli orbitali molecolari ed atomici con le caratteristiche di simmetria degli OM.
Per gli OA la simmetria è rispetto al nucleo, per gli OM rispetto all'asse di legame.
Gli OM antileganti s*, p*, d* hanno in più un piano nodale perpendicolare all'asse di legame: mentre i Yb hanno alta densità elettronica fra i due nuclei (non necessariamente "lungo" l'asse di legame), i Ya hanno, nella stessa zona, densità trascurabile.
Infatti la densità elettronica o la probabilità di trovare un elettrone in uno spazio, si ottiene dal quadrato della funzione d'onda dell'OM:
Yb2 = yA2 + 2yAyB + yB2 Ya2 = yA2 - 2yAyB + yB2
La differenza fra i due è il termine centrale, detto integrale di sovrapposizione: S = ò 2yAyB dt
| Fig.15.3
Integrali di sovrapposizione tra orbitali atomici diversi. Nella parte in alto del disegno, due esempi di sovrapposizione di orbitali p, con integrale superiore a zero, S>0: la densità elettronica fra i due nuclei aumenta (Yb) e si forma un legame. Nella parte centrale, due esempi di sovrapposizione di orbitali p, con integrale inferiore a zero, S<0: la densità elettronica fra i due nuclei diminuisce (Ya) e si forma un antilegame. Nella parte in basso, un esempio di sovrapposizione di un orbitale s con un orbitale p, con integrale eguale a zero, S=0: l'integrale positivo dovuto alla sovrapposizione delle due parti degli orbitali con segno eguale viene esattamente annullato dall'integrale negativo dovuto alla sovrapposizione delle due parti degli orbitali con segno opposto. Non esiste alcuna interazione; è una situazione di "non legame".
|
 |
Perché possa esserci un buon legame covalente sono necessarie varie condizioni, che matematicamente sono rappresentate, per esempio, dall'integrale di sovrapposizione; occorre che non sia possibile il legame ionico (i due atomi devono avere elettronegatività abbastanza simile); occorre che le energie degli elettroni in A e in B siano abbastanza vicine; la sovrapposizione degli OA deve essere sufficiente; la repulsione fra elettroni deve essere minima; gli OA devono avere la stessa simmetria rispetto all'asse A-B...
Per molecole biatomiche omonucleari del 2° periodo abbiamo a disposizione anche gli OA p; avremo perciò più OM.
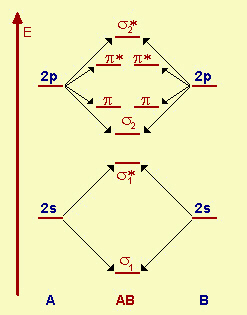
| Fig.15.4
Schema energetico di formazione di OM partendo dagli OA dei due atomi A e B quando A e B
sono omonucleari (stessi atomi). Il fatto che A e B siano due atomi uguali è dimostrato dallo stesso livello energetico per i 2s e i 2p dei due atomi. I 2p sono 3 orbitali degeneri perciò alla stessa E. Essendo in totale 6, danno luogo a 6 OM, un s e un s* lungo l'asse internucleare, 2 p e 2 p* fuori dall'asse. La collocazione degli elettroni disponibili avviene sempre sulla base dell'aufbau, occupando progressivamente gli orbitali a più bassa energia e ricordando che in ogni OM non possono coesistere più di due elettroni e questi devono essere a spin antiparallelo. Il s derivato dai p potrà essere così impegnato solo quando siano completati s e s* derivati dai 2s (con un annullamento dell'effetto di legame). |
 |
Se ci fossero anche le condizioni per l'ibridazione, per esempio sp2, gli OA di partenza sarebbero alla stessa E e si avrebbe un solo s (e un solo s*).
Poiché la sovrapposizione per i p perpendicolari all'asse è minore che per quelli coassiali (perciò i legami conseguenti provocano una minore stabilizzazione), la DE relativa a p-p* è minore che per s2-s2*.
molecola |
configurazione |
ordine di legame |
E legame (kJ mol-1) |
distanza (pm) |
H2 |
s12 | 1 |
432 |
74 |
He2+ |
s12 s1*1 | 0,5 |
||
He |
s12 s1*2 | 0 |
- |
- |
Li2 |
s12 | 1 |
105 |
267 |
Be |
s12 s1*2 | 0 |
- |
- |
B2 |
s12 s1*2 s22 | 1 |
289 |
159 |
C2 |
s12 s1*2 s22 p2 | 2 |
628 |
131 |
N2 |
s12 s1*2 s22 p4 | 3 |
942 |
110 |
O2 |
s12 s1*2 s22 p4 p*2 | 2 |
494 |
121 |
F2 |
s12 s1*2 s22 p4 p*4 | 1 |
151 |
142 |
Ne |
s12 s1*2 s22 p4 p*4 s2*2 | 0 |
- |
- |
Fig.15.5 Configurazioni elettroniche, energia e distanza di legame per alcuni sistemi binucleari omonucleari. Per boro B, e carbonio C, la situazione è più complessa (interazioni fra il 2s di un atomo e il 2p dell'altro, con E diverse; lo trascuriamo in prima approssimazione). Per l'ossigeno O, ci sono 2 elettroni in due orbitali degeneri p*, perciò essi sono a spin parallelo: cio è causa del paramagnetismo reale della molecola O2.
Per molecole biatomiche eteronucleari, poiché le energie degli OA dei due nuclei sono diverse, il diagramma risulta asimmetrico.
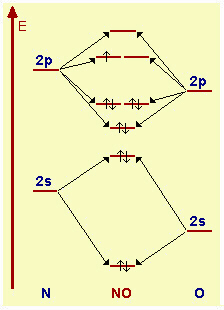
| Fig.15.6
Schema energetico di formazione degli OM per la molecola di monossido di azoto, NO. Nella formazione della molecola NO partendo da un atomo O e un atomo N, gli OA di O sono a E più bassa, poiché O ha carica nucleare maggiore di N. L'ordine di legame risultante è di 2.5 (3 coppie di elettroni, indicati dalle coppie di elettroni con spin antiparalleli, negli OM di legame, 0.5 in quelli di antilegame p*, corrispondente all'elettrone sul primo orbitale di antilegame p*. Questo avviene poiché il sistema ha 11 elettroni (6 per O, 5 per N). L'ordine di legame sarebbe invece 2 per NO- (12 elettroni); un secondo elettrone a spin spaiato occuperebbe infatti il secondo orbitale di antilegame p*. L'ordine di legame sarebbe 3 per NO+ (10 elettroni); in questo ione, infatti, nessun elettrone si troverebbe negli orbitali di antilegame p*. |
 |
Per molecole poliatomiche il problema diventa ancora più complesso, poiché diventa essenziale, vista la geometria delle molecole, tener conto non di OA puri, ma di quelli ibridi (come avviene, per esempio, in H2O, NH3...): le sovrapposizioni sono più difficilmente valutabili e si hanno differenze di E consistente fra i vari OM.
Per costruire gli OM è necessario, in questi casi, partire dagli ibridi; se restano doppietti liberi (elettroni non impegnati in legami), è chiaro che bisogna considerare anche questi, che potranno essere, in generale, a energia vicina a quella degli OA prima della formazione degli OM.
Abbiamo visto che esiste una vasta gamma di legami covalenti polari compresi fra i due estremi, il legame ionico e il legame covalente puro o omeopolare.
Possiamo così analizzare i vari legami secondo uno dei due modelli indifferentemente, anche se è utile usare il modello che più si avvicina alle caratteristiche del legame in questione; anche se si partisse, però, dal modello sbagliato, si potrebbe giungere alle stesse conclusioni, effettuando successive correzioni e approssimazioni: il lavoro sarebbe soltanto più lungo.