Corso di chimica generale ed inorganica
Vai all'INDICE GENERALE
23 - l'acqua
Gli equilibri in soluzione acquosa sono
particolarmente importanti in molti sistemi chimici e in tutti i sistemi biologici e
geologici. E' essenziale perciò conoscere alcune caratteristiche dell'acqua, fondamentali
per la comprensione di buona parte dei processi che riguardano l'uomo e l'ambiente in cui
vive.
L'acqua, allo stato liquido, è
costituita da agglomerati di molecole unite da legami di idrogeno, in una situazione
dinamica, in cui cioè i legami di idrogeno
si formano e si rompono continuamente.
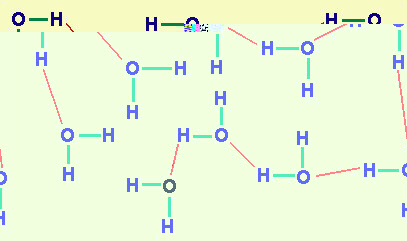
| Fig.23.1
Rappresentazione schematica planare di molecole di acqua con legami di idrogeno. Nel disegno i legami OH di ogni molecola appaiono,
per semplicità, disegnati a 90° tra loro (sappiamo che non è vero!); in verde i legami
covalenti normali; in rosso i legami a idrogeno.
Quanto più questi ultimi sono lunghi,
tanto più essi sono allentati, perciò o si stanno formando o si stanno rompendo.
Quando un legame di idrogeno si forma, si
possono allentare quelli covalenti preesistenti, che si possono rompere a loro volta, in
una situazione di totale dinamicità. |
 |
Una piccola parte
delle molecole è dissociata secondo la reazione
H2O ¨ H+ + OH-
Questa scrittura è una approssimazione
semplicistica, poiché, in realtà, questi ioni (come tutti gli ioni in soluzione
acquosa!) sono "solvatati" da altre molecole di acqua; sono cioè praticamente
circondati dalla parte polare delle molecole circostanti che è di segno opposto rispetto
alla carica dello ione.
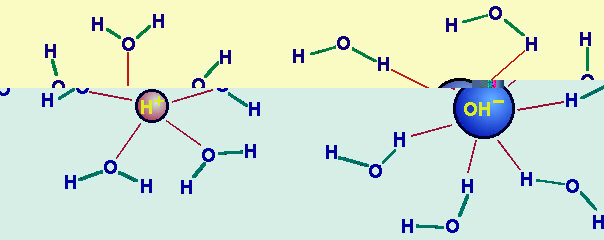
| Fig.23.2
Rappresentazione schematica planare della solvatazione degli ioni H+ e OH-
da parte di molecole di acqua.
Il tratto sottile in rosso rappresenta
legami relativamente deboli di interazione elettrostatica. |
 |
In pratica potremmo scrivere, per
esempio, in base alla figura,
12 H2O ¨ H11O5+
+ H13O7-
ma, non potendo conoscere esattamente il
numero di molecole coinvolte, non sarebbe possibile scrivere una formula corretta.
Per semplicità e per convenzione
scriviamo perciò
2 H2O ¨ H3O+ +
OH-
in cui H3O+ =
ione idrossonio
e OH- = ione ossidrile
L'equilibrio ha
ovviamente una sua costante, ma poiché l'attività di H2O è costante, essa
può venire conglobata nella costante di
equilibrio e si ottiene così:
K [H2O] = [H3O+] [OH-] = Kw
Questa Kw, che si
chiama prodotto ionico dell'acqua, a 25°C, vale
(Kw)25°C = 1.00 x 10-14 mol2 dm-6
Nell'acqua pura è ovviamente [H3O+]
= [OH-] = 10-7 mol dm-3
La Kw aumenta
all'aumentare della T, poiché la reazione di dissociazione è endotermica (trascurando la
solvatazione); per esempio, a 50°C
(Kw)50°C = 5,47 x 10-14 mol2 dm-6
Questo significa che in acqua pura, a
50°, la [H3O+] è maggiore che a 25°.
Se, restando in soluzioni abbastanza
diluite, introduciamo in acqua n moli di un acido forte HA, questo si dissocia
completamente in ioni (poiché è "forte"): gli ioni H+,
solvatati, danno n moli di H3O+ e, analogamente, di A-.
Lo stesso succede con n moli di base
forte BOH, da cui avremo n moli di OH- e di B+.
In ogni caso viene modificato il rapporto
esistente nell'acqua pura tra H3O+ e OH-.
Potremo ricavare, mediante calcoli
semplicissimi, le concentrazioni relative dalla Kw, dato che essa, a una
data T, è costante (il prodotto ionico dell'acqua è direttamente derivato da una
costante termodinamica!).
Per i chimici (e biologi, microbiologi,
biochimici, medici, geologi, ecc.) è fondamentale definire una unità di misura
dell'acidità delle soluzioni, cioè della [H3O+]. Poiché è
scomodo usare numeri molto piccoli o esponenziali in base 10, preferiamo utilizzare una nuova
unità di misura, il pH.
p rappresenta l'operatore
matematico -lg, perciò
pH = -lg [H3O+]
Il pH è definito perciò come il logaritmo
decimale della concentrazione molare degli ioni idrogeno, con segno negativo. Lo
stesso operatore p è ovviamente applicabile a qualunque grandezza la cui misura sia
esprimibile come un esponenziale in base 10.
Poiché è Kw = [H3O+]
[OH-], allora pKw(25°C) = pH + pOH = 14
E' utile allora definire una scala
per pH e per pOH (che sono d'altronde legate attraverso il pKw)
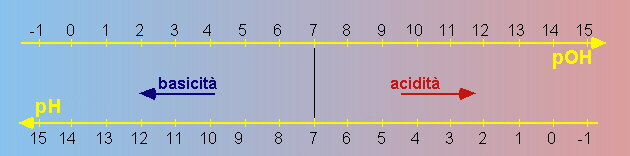
Fig.23.3 Scale di pH
e di pOH, cioè di acidità e basicità. pH = pOH = 7 corrisponde alla
neutralità. La somma pH+pOH = 14 in ogni soluzione acquosa a 25°C. Da notare che le
scale non iniziano da 0 e non terminano a 14: questi valori corrispondono semplicemente a
soluzioni che contengano 1 sola mole/litro di acido o base forte; è facile ottenere
soluzioni acide con pH<0 (una soluzione che contenga 10 moli/litro di HCl ha infatti pH
= -1 e pOH = 15).


