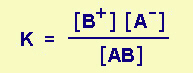Corso di chimica generale ed inorganica 25 - equilibri eterogenei Fino ad ora abbiamo
trattato soluzioni acquose, che sono sistemi omogenei, ma talvolta si presentano anche
sistemi eterogenei in cui sono coinvolti equilibri eterogenei, molto importanti
nella chimica analitica; generalmente questi sono legati alla presenza di sali poco
solubili che, in quanto sali, sono sempre elettroliti forti (tanto più che la loro
solubilità è molto bassa). Consideriamo un sale poco solubile AB:
questo si dissocia:
AB ¬® A- + B+ ma poiché il sale poco solubile è
presente come corpo di fondo, la sua concentrazione [AB] (o meglio la sua
attività) è costante, perciò
K [AB] = [A-] [B+] = KPS KPS è chiamato prodotto
di solubilità; essendo derivato da una K di equilibrio, è anch'esso una costante, a
T costante, purché sia presente il sale come corpo di fondo (altrimenti non potremmo
conglobare la sua attività nella costante). KPS è strettamente
legato alla solubilità s del sale (ricordiamo che solubilità =
quantità massima del sale che può essere sciolta in una data quantità di solvente a una
certa T). Poiché i sali sono elettroliti forti, la
loro concentrazione in forma indissociata è costante ma assolutamente trascurabile:
perciò la concentrazione degli ioni è ricavabile dalla solubilità del sale. Se consideriamo un sale generico BnAm
e ricordando che (s) significa solido, (aq) significa in soluzione acquosa, si
possono individuare gli equilibri indicati in figura: Fig.25.1 Equilibri di un
sale poco solubile in fase solida, in soluzione acquosa, in forma ionizzata Praticamente si fa
riferimento all'equilibrio indicato con le frecce in rosso, data l'osservazione
precedente; l'attività del sale è condizionata dalla presenza del sale come corpo solido
in fase eterogenea rispetto alla soluzione, perciò alla sua solubilità s. Prendiamo come esempio il
fosfato tricalcico:
Ca3 (PO4)2 (s) ¨ 3 Ca2+
+ 2 PO43- KPS =
[Ca2+]3 [PO43-]2
= (3s)3 (2s)2 = 27 x 4 x s5 E' ovvia la necessità di usare i
logaritmi in questi casi! Volendo infatti ricavare la solubilità
s conoscendo la KPS, si avrà:
s = (KPS /108)1/5 e passando ai logaritmi
lg s = 1/5 lg KPS - 1/5 lg 108 Sono noti i prodotti di
solubilità di moltissimi sali poco solubili; per alcuni si tratta di valori
veramente bassissimi (se si ricorda che la costante di Avogadro è circa 6x10-23,
si può calcolare che, per esempio per HgS, la solubilità è di 1 molecola in poco meno
di 10.000 litri di soluzione!). Si riportano, nella tabella, alcuni
valori significativi di prodotti di solubilità a 25°C. sale KPS sale KPS sale KPS CaSO4 2,4x10-5 BaSO4 1,1x10-10 FeS 3,7x10-19 SrCrO4 3,6x10-5 AgCl 1,6x10-10 ZnS 1,2x10-23 Ca(OH)2 1,3x10-6 Ag2CrO4 1,2x10-12 PbS 3,4x10-28 BaF2 1,7x10-6 AgBr 7,7x10-13 Ag2S 1,6x10-49 PbSO4 1,8x10-7 AgCN 1,6x10-14 HgS 1,6x10-54 CaCO3 8,7x10-9 AgI 1,5x10-16 Fig.25.2 Prodotti di solubilità di
alcuni sali. La conoscenza dei prodotti di solubilità
(e della solubilità) ha molta importanza sia in chimica analitica (molte determinazioni
qualitative e quantitative sfruttano queste caratteristiche) sia in chimica applicata
(basti pensare ai problemi del degrado dei materiali lapidei calcarei e agli interventi
per il restauro). In particolare è interessante notare che
dalla KPS del carbonato di calcio, costituente principale dei marmi, si
può calcolare una solubilità di circa 9x10-5, mentre da quella del
solfato di calcio, prodotto del degrado dei marmi a causa delle piogge acide, si ricava
una solubilità di circa 5x10-3, cioè quasi 60 volte maggiore: per tale
ragione, quando il carbonato viene trasformato in solfato dall'acido solforico trasportato
dall'acqua piovana, parte del materiale viene dilavato. E questo è solo un esempio. Ma se alla soluzione di un sale poco
solubile viene aggiunto uno degli ioni costituenti il sale, che cosa succede? Poiché a quella T, il KPS
è costante, dovrà diminuire la concentrazione dell'altro ione (e dovrà precipitare,
cioè separarsi dalla soluzione, una certa quantità di sale). Questo è detto effetto
dello ione comune ed è una conseguenza del principio
di Le Chatelier. Prendiamo per esempio una soluzione di
cloruro d'argento AgCl:
[Ag+] [Cl-] = 1,6 x 10-10 perciò
[Ag+] = [Cl-] = (1,6 x 10-10)1/2 = 1,265 x
10-5 Se ora aggiungo Cl-
(per esempio sotto forma di NaCl) in concentrazione 10-2 M,
avremo: [Ag+] [Cl-] = [Ag+]
(10-2 + 1,265 x 10-5) = 1,6 x 10-10 [Ag+] = 1,6 x 10-10/10-2
= 1,6 x 10-8 La concentrazione di Ag+ deve
perciò ridursi di molto; precipiterà, sotto forma di AgCl tutto quello
che è in eccesso. Questo effetto viene utilizzato, per
esempio, per ridurre la concentrazione di ioni pericolosi nelle acque di scarico
industriali.