Corso di chimica generale ed inorganica 28 - gli equilibri tra le fasi La regola č molto
semplice: v = c + 2 - f v = varianza o gradi di libertŕ; rappresenta il
numero di variabili fisiche o chimiche che č possibile modificare senza che nel sistema
scompaiano una o piů fasi c = numero di componenti
indipendenti del sistema f = numero di fasi 2 = corrisponde alle
due variabili pressione p e temperatura t Fig.28.1 Josiah Willard Gibbs Consideriamo un
sistema a un solo componente, come l'acqua. Misuriamo le coppie
di parametri p e t a cui l'acqua si presenta nelle sue varie fasi: solida, liquida,
gassosa; quindi portiamo questi dati in un grafico p/t. Questo grafico si
chiama diagramma di stato. Ogni sostanza ha
il suo e rappresenta le condizioni di p e t in cui sono possibili i vari equilibri tra le
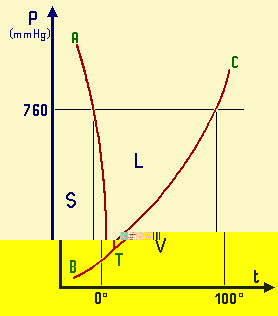
fasi della sostanza e le loro condizioni di esistenza. S
= zona di esistenza della fase solida L = zona di esistenza della fase liquida V = zona di esistenza della fase vapore BT = curva di coesistenza delle fasi
solido-vapore; corrisponde al processo di sublimazione TC = curva di coesistenza delle fasi
liquido-vapore; corrisponde ai processi di evaporazione-condensazione TA = curva di coesistenza delle fasi
solido-liquido; corrisponde ai processi di fusione-solidificazione T = punto triplo di coesistenza delle
fasi solido-liquido-vapore Il punto
triplo T
č caratterizzato da una unica coppia di valori per p e per t: 4,58
mm Hg e 0,01°C. Esso non coincide
col punto di fusione (p 760 mmHg; t 0,00°C), poiché questa avviene in presenza di una p
esterna, esercitata dall'aria, come evidenziato nel diagramma. La curva TA rappresenta cosě
la variazione del punto di fusione sotto l'effetto di una p esterna. Ovviamente, sopra al
punto critico (temperatura critica 374°C, pressione
critica 218 atm) non puň esistere
equilibrio liquido-vapore L-V, poiché l'acqua esiste solo allo stato vapore. L'inclinazione di
TA verso sinistra, al crescere della pressione, fa capire che, se aumento la p su ghiaccio
a 0°C, questo fonde (questo fenomeno viene sfruttato, per esempio, nel pattinaggio sul
ghiaccio: la pressione esercitata dalle lame del pattino provocano una fusione
superficiale del ghiaccio: il velo d'acqua liquida permette un piů facile scorrimento
della lama sul ghiaccio; quando la pressione torna al livello normale, il velo di acqua
solidifica nuovamente). Esaminiamo il
diagramma con la regola delle fasi: Fig.28.3 Analisi del diagramma di
stato dell'acqua mediante la regola delle fasi Possiamo cioč
cambiare sia pressione sia temperatura (entro certi limiti) senza che, nel sistema, cambi
il numero delle fasi, nel bivariante; una sola delle variabili nel monovariante
(determinata una variabile, l'altra č condizionata); non possiamo cambiarne alcuna delle
due nell'invariante (altrimenti si esce dalle condizioni del punto triplo). Esaminiamo il caso
analogo dell'anidride carbonica o diossido di carbonio, CO2 S = zona di esistenza della fase solida L = zona di esistenza della fase liquida V = zona di esistenza della fase vapore E = punto di sublimazione del
"ghiaccio secco" (p = 1 atm; t = -78°C) T = punto triplo di coesistenza delle tre
fasi (p = 5.2 atm; t = -57°C) Se scaldiamo CO2 solida (ghiaccio
secco) a p ambiente (1 atm), essa sublima senza passare allo stato liquido: infatti
l'equilibrio liquido-solido esiste solo per p > 5,2 atm. Alcuni sistemi
monocomponente sono perň piů complessi, come succede per lo zolfo, S B = punto triplo di coesistenza delle fasi Sa-Sb-vapore (p 0.01 mm Hg; T 95.5°C) C = punto triplo di coesistenza delle
fasi Sb-liquido-vapore (p 0.025 mm Hg; T 119°C) F = punto triplo di coesistenza delle
fasi Sa-Sb-liquido
(p 1290 atm; T 151°C) H = punto metastabile (T 113°C) AB = curva corrispondente alla
sublimazione di Sa BC = curva corrispondente alla
sublimazione di Sb CD = curva corrispondente
all'evaporazione dello zolfo liquido BF = curva corrispondente alla
transizione solido-solido Sa-Sb CF = curva corrispondente alla
fusione-soldificazione di Sb S, allo stato
solido, esiste, in natura, in due forme cristalline allotropiche (che si trasformano l'una
nell'altra in base alle condizioni ambientali): la forma a, rombica, č
stabile fino a 95,5°C; la b, monoclina, da
95,5° a 119°C, che č la T di fusione. Quando t=95,5°C, S passa dalla forma a alla
In un sistema
eterogeneo lo stato di equilibrio č prevedibile con la regola delle fasi, enunciata dal
chimico fisico americano Josiah
Willard Gibbs (1839-1903) in
base a considerazioni termodinamiche.

Fig.28.2
Diagramma di stato dell'acqua (p/t). Il diagramma non č in scala (dovrebbe essere molto
piů allungato verso l'alto, ma se cosě fosse, non sarebbe evidente la curvatura di TA
verso temperature basse.
al punto triplo T
v = 1 + 2
- 3 = 0
sistema
invariante
lungo le curve BT,
TC, TA
v = 1 + 2
- 2 = 1
sistema
monovariante
entro le aree S, L,
V
v = 1 + 2
- 1 = 2
sistema
bivariante
Fig.28.4
Diagramma di stato (p/t) del diossido di carbonio o anidride carbonica.
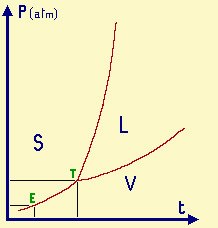
Fig.28.5
Diagramma di stato p/t per lo zolfo.
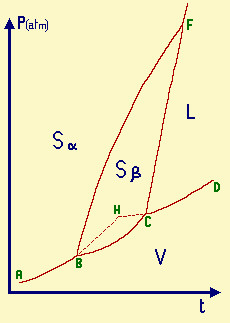
Fig.28.6
Cristalli di zolfo rombico Sa a destra e di zolfo monoclino Sb in basso


Raffreddando lentamente S liquido si hanno i processi inversi (enantiotropia); poiché perň le trasformazioni in fase solida sono lentissime, se raffreddiamo velocemente S liquido, questo cristallizza a 113°C nella forma b instabile, che lentamente si trasforma in a. Analogamente, se scaldiamo velocemente Sa, questo fonde a 113°C, senza passare dalla forma b (punto H).
Sopra al punto F, Sa fonde direttamente, senza passare per la forma b: perciň il polimorfismo di S non esiste a p>1290 atm.
La regola delle fasi č utilizzabile in modo analogo al caso dell'acqua. Non č possibile la coesistenza delle 4 fasi (avremmo v=-1).
Passiamo ai sistemi a due componenti; possono essere di diversi tipi, che possiamo considerare "soluzioni" (non sono ovviamente indicate piů volte quelle dello stesso tipo: per esempio S + L, dato che esiste la L + S, ecc.)
"soluzione" |
componenti |
componenti |
componenti |
solida S |
S + S |
- |
S + G |
liquida L |
L + S |
L + L |
L + G |
gassosa G |
- |
- |
G + G |
Fig.28.7 Schema dei possibili accoppiamenti di fasi diverse nella formazione di una "soluzione", e suo stato fisico possibile.
Le piů comuni sono quelle in fase liquida, in cui si considera un "solvente" e un "soluto"; quest'ultimo puň essere volatile (L + G, oppure L + L) o non volatile (L + S).
Il chimico fisico francese François Marie Raoult (1830-1901) ha studiato il comportamento delle soluzioni L + L in funzione della t e della p.
Dalle sue esperienze ha dedotto che, ad una t prefissata, la tensione di vapore di un componente č proporzionale alla sua frazione molare.
Consideriamo una soluzione di due componenti liquidi, A e B, completamente miscibili tra loro.
| Fig.28.8
Diagramma isotermo liquido-vapore (L-V) di un sistema ideale bicomponente A e B. T = costante L = zona di esistenza della fase liquida V = zona di esistenza della fase vapore p°A = tensione di vapore di A p°B = tensione di vapore di B c A = frazione molare di A cB = frazione molare di B |
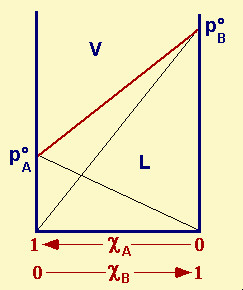 |
La pA, proporzionale alla frazione molare cA, parte ovviamente da 0 quando cA=0, e arriva a pA° quando cA=1; pB, proporzionale a cB, va in senso opposto.
| Fig.28.9
John Dalton (1766-1844), uno dei padri della chimica
Per la legge di Dalton sui miscugli gassosi, la pressione totale del sistema č Ptot = pA + pB = cApA° + cBpB° Questa relazione dice praticamente che, per la pressione totale Ptot, consideriamo il segmento pA°-pB°, dovuto appunto alla somma, punto per punto, dei contributi della p dei due componenti. Questo č interpretabile pensando che, poiché l'evaporazione avviene dalla superficie, quanto maggiore č il numero di particelle di una specie sulla superficie, tanto maggiore č la sua p parziale. |
 |
In effetti anche questa č una legge ideale, valida per soluzioni in cui le molecole dei due componenti interagiscono tra loro come le molecole della stessa specie; cioč quando le interazioni A-A = B-B = A-B
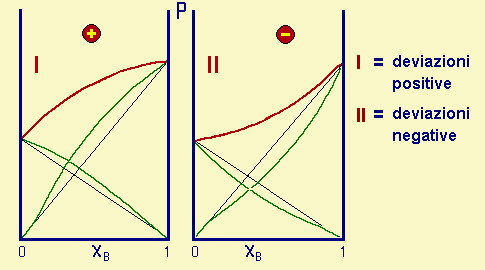
In realtŕ possiamo avere deviazioni positive (esempio I), quando le attrazioni A-B sono minori delle A-A e delle B-B: in tal caso, infatti, le molecole possono liberarsi piů facilmente, creando perciň una p maggiore.
Oppure, benché piů raramente, deviazioni negative (esempio II), corrispondenti ad attrazioni A-B maggiori sia delle A-A sia delle B-B.
| Fig.28.10
Diagrammi isotermi liquido-vapore L-V per sistemi reali, con deviazioni positive (es.
etere e acetone) e negative (es. acido acetico e piridina) rispetto all'ideale. In ascissa la frazione molare di B; in ordinata la tensione di vapore p. In nero la tensione di vapore ideale dei due componenti A e B. In verde la tensione di vapore reale dei componenti A e B, con le rispettive deviazioni. In rosso la curva risultante dalla somma dei contributi reali dei due componenti, corripondente alla tensione di vapore reale della soluzione di A e B. |
 |
In generale, il vapore in equilibrio con una miscela binaria di due liquidi volatili, č piů ricca nel componente piů volatile: questa č detta regola di Konowaloff.
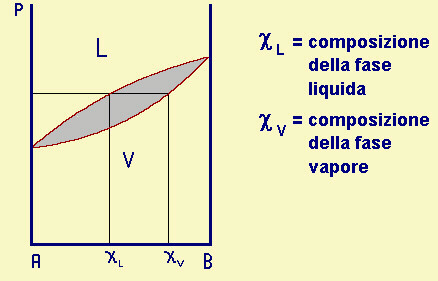
| Fig.28.11
Diagramma L-V isotermo per un sistema bicomponente reale. Le due curve rappresentano la composizione del liquido, e del vapore in equilibrio con esso, alle varie temperature (ad ogni temperatura corrisponderŕ cioč un diagramma di questo tipo, ma con valori diversi di p). I punti dell''area compresa tra le due curve (in grigio) non hanno significato fisico: non esiste un sistema in quelle condizioni, poiché esso si smista in un liquido di composizione cL e un vapore di composizione cV. La composizione delle fasi liquido e vapore, all'equilibrio, sono diverse, come indicato dalle frazioni molari cL e cV rappresentate in figura. |
 |
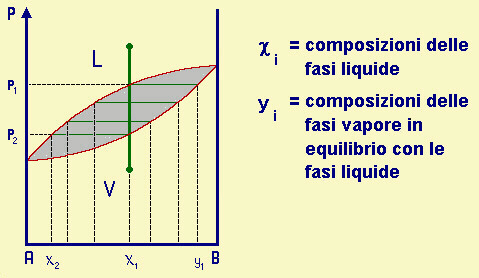
Cerchiamo di capire che cosa succede se, partendo da una soluzione (A+B) di composizione c1, diminuiamo la pressione del sistema, mantenendo la temperatura costante (consideriamo perciň un diagramma isotermo):
| Fig.28.12
Diagramma isotermo che rappresenta la distillazione di una soluzione bicomponente in
funzione della pressione. Il punto di partenza č indicato dal punto verde in alto, quello
di arrivo dal punto verde in basso. A p=p1 la soluzione di composizione c1 č in equilibrio col vapore di composizione y1; poiché questo č piů ricco in B, la soluzione si impoverisce di B e la sua composizione segue gradualmente la curva verso sinistra, con una riduzione della p per l'evaporazione. Ad ogni composizione ci della soluzione corrisponde una composizione yi del vapore; a p=p2 si ha totale evaporazione della fase liquida con composizione c2; a questo punto il vapore ha la composizione c1. |
 |
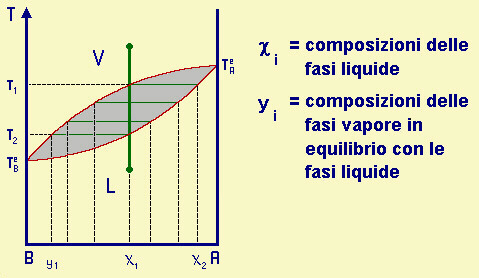
Quando si parla di distillazione frazionata, si preferisce usare un diagramma isobaro anziché isotermo, dato che normalmente si opera a p atmosferica; in questo caso, invece delle tensioni di vapore, avremo le T di ebollizione. Il punto di partenza č lo stesso, ma, dato che a tensione di vapore piů alta corrisponde temperatura di ebollizione piů bassa, il diagramma presenta a sinistra B e a destra A (la frazione molare di B aumenta da sinistra a destra); inoltre, ovviamente, la zona in alto corrisponde alla fase vapore, quella in basso alla fase liquida.
| Fig.28.13
Diagramma isobaro della distillazione frazionata di un sistema bicomponente A-B. Il punto di partenza č indicato dal punto verde in basso, quello di arrivo dal punto verde in alto. TA° = temperatura di ebollizione di A puro TB° = temperatura di ebollizione di B puro Ti = temperatura di ebollizione delle soluzioni i La soluzione iniziale (e il vapore finale) ha composizione c1; quando inizia la distillazione il vapore ha composizione y1; quando finisce, la soluzione ha composizione c2. |
 |
Con la distillazione frazionata č possibile recuperare (facendole condensare) frazioni di vapore piů ricche in B e frazioni di liquido piů ricche in A; operando poi sulle frazioni, č possibile avvicinarsi sempre piů, ma senza mai raggiungerle, a frazioni sempre piů ricche in A o in B.
In alcuni casi accade che alcune miscele di liquidi, di composizione definita, distillino completamente ad una temperatura costante, come se fossero liquidi puri: queste miscele si chiamano miscele azeňtrope.
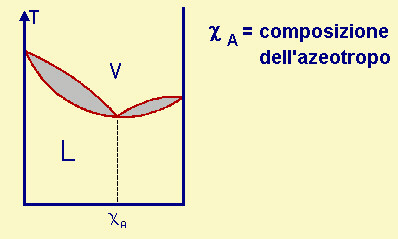
| Fig.28.14
Diagramma isobaro di distillazione di un sistema binario A-B in cui A e B danno una
miscela azeotropa di composizione cA. A destra e a sinistra della composizione azeotropica il comportamento č analogo a quello descritto in precedenza (come se il diagramma fosse costituito da due diagrammi a lente affiancati, uno con componenti A puro e cA, l'altro con componenti cA e B puro. Se perň si cambia p, puň cambiare la composizione azeotropica. |
 |
Per esempio, nel caso della miscela EtOH/H2O:
P (mm Hg) |
% EtOH |
% H2O |
760 |
96,3 |
3,7 |
9,5 |
99,5 |
0,5 |
Fig.28.15 Variazioni dell'azeotropo etanolo/acqua con la pressione
Se ne deduce che č impossibile ottenere comunque EtOH puro per distillazione di miscele EtOH/H2O a pressione atmosferica, ma anche a p diverse; per poter ottenere EtOH puro occorre "rompere" l'azeotropo aggiungendo un altro componente che faccia, con H2O, un azeotropo a T di ebollizione piů basso (come il benzene).
Molte coppie di sostanze danno miscele azeotropiche (e molte danno anche azeotropi ternari).
A |
B |
(Teb)A |
(Teb)B |
(Teb)azeo |
% A |
EtOH |
H2O |
78,5 |
100,0 |
78,2 |
96,3 |
C6H6 |
EtOH |
80,0 |
78,5 |
66 |
67,45 |
n-ProOH |
H2O |
97,2 |
100,0 |
87,7 |
71,7 |
HCl |
H2O |
-83,7 |
100,0 |
110 |
20,1 |
MeOH |
CH3COCH3 |
64,7 |
56,5 |
56 |
86,5 |
EtOH |
CCl4 |
78,5 |
76,8 |
65 |
15,8 |
Fig.28.16 Esempi di coppie di sostanze che danno miscele azeotrope; punti di ebollizione delle sostanze pure e degli azeotropi a 760 mmHg; percentuale del componente A nella miscela azeotropa.
Esistono anche sistemi in equilibrio solido-vapore, come il sistema solfato di rame/acqua, CuSO4/H2O: per esso sono possibili tre forme idrate del sale, e gli equilibri tra le varie forme sono facilmente interpretabili secondo la regola delle fasi
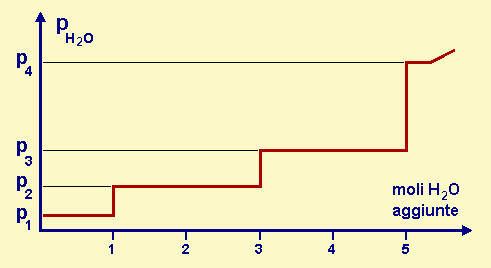
| Fig.28.17
Diagramma isotermo pressione/moli di H2O vapore aggiunte per il sistema CuSO4/H2O.
Il sistema č costituito da 1 mole di CuSO4 e le reazioni relative sono: CuSO4(s) + H2O (g) ¬® CuSO4H2O(s) CuSO4H2O(s) + 2H2O (g)¬®CuSO43H2O(s) CuSO43H2O(s)+ 2H2O(g) ¬®CuSO45H2O(s) A titolo informativo (le p non sono in scala): p2 = 0,8 mm Hg; p3 = 7,8 mmHg. |
 |
Le componenti indipendenti sono sempre 2 (le altre sono strettamente legate mediante gli equilibri indicati nella didascalia della figura), le fasi (considerando uno qualsiasi degli equilibri) sempre 3, perciň ogni sistema corrispondente alle reazioni indicate č monovariante:
v = 2 + 2 - 3 = 1
Introduciamo lentamente vapore d'acqua in un recipiente chiuso contenente 1 mole di CuSO4.
La p di H2O cresce fino a p1; ora la p rimane costante finché tutto il CuSO4 si č trasformato in CuSO4H2O.
Poi p aumenta fino a p2; ora p resta costante finché tutta la fase si č trasformata nella fase CuSO43H2O..., etc. Ciň avviene perché, quando sono presenti 2 fasi solide, (con H2O vapore sono 3), essendo T=cost., la p non puň variare, finché le fasi non tornano ad essere solo 2, una solida e una gassosa; solo a queste condizioni il sistema č bivariante.
Quando si č giunti a CuSO45H2O, l'aggiunta di H2O (sempre come vapore) porta alla dissoluzione del pentaidrato: entra in gioco una nuova fase, liquida; il sistema ridiventa monovariante e la p resta eguale a p4.
Quando perň il solido č tutto disciolto, le fasi sono solo 2, (soluzione e vapore): la p di H2O puň perciň aumentare, tendendo alla tensione di vapore dell'acqua a quella temperatura.
Per sistemi binari liquido-gas (2 componenti, 2 fasi),
v = 2 + 2 - 2 = 2
Il sistema č bivariante: dei 3 parametri (p, T, composizione), possiamo definirne solo 2, il terzo č conseguente.
Il chimico fisico inglese William Henry (1715-1836) ha dedotto la legge omonima
[gas] = K pgas
La solubilitŕ di un gas in un solvente con cui non reagisce, ad una data T, č proporzionale alla pressione parziale del gas sopra la soluzione.
In generale la solubilitŕ dei gas nei liquidi diminuisce con l'aumentare della temperatura.