Corso di chimica generale ed inorganica 18 - i gas Le particelle gassose hanno energia
cinetica maggiore dell'energia di attrazione, perciò tendono ad occupare tutto
lo spazio disponibile. Lo stato gassoso possiede diverse proprietà: 2 proprietà estensive:
massa, volume 2 proprietà intensive:
temperatura, pressione Queste proprietà compaiono nella equazione
di stato dei gas perfetti o ideali P V = n R T in cui P rappresenta la
pressione, V il volume, n il numero di moli, T
la temperatura assoluta e R la costante universale dei gas
che dipende dalle unità di misura usate per
le variabili. Per esempio:
R = 0.082 dm3 atm mol-1
K-1 R = 8.3143 J mol-1 K-1 Questa legge comprende altre leggi che
prendono in considerazione il comportamento dei gas mantenendo fissa una delle variabili: • Legge di Boyle (isoterma,
cioè a T costante) (PV)T
= K • Legge di Charles-Gay Lussac
(isobara, cioè a P costante) (V)p = Vo (1+aot)
in cui: V0 è il volume occupato a 0°C; a0 = 1/273.15; t, temperatura, è espressa in °C.
Se poniamo t = -273.15, allora V = 0. Tale t è presa come punto di zero della scala assoluta, cioè -273.15°C, corrispondente a 0 K (Kelvin).
• Principio di Avogadro: volumi eguali di gas diversi, alle stesse T e P, contengono lo stesso numero di particelle.
Perciò il volume di un gas può essere usato come misura della quantità, poiché è proporzionale al numero di moli di gas.
Questo principio, enunciato nel 1811, era così rivoluzionario, che dovettero passare 50 anni, prima che fosse accettato (nel I° Congresso Internazionale di Chimica a Karlsruhe), per merito di Cannizzaro, che ne comprese l'importanza.
La legge generale dei gas si applica correttamente solo al gas ideale o perfetto, costituito di particelle tutte uguali, con la stessa massa e con volume nullo (puntiformi): è un modello che è stato costruito per razionalizzare il comportamento dei gas.
Un gas reale è invece caratterizzato da particelle con un volume definito; se si vuole perciò applicare la legge dei gas a gas reali è necessario introdurre delle correzioni.
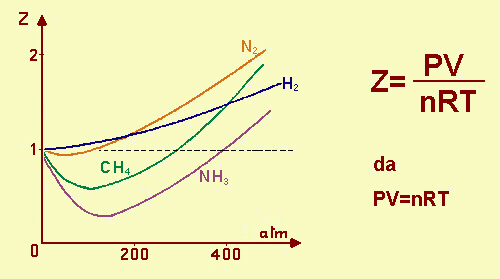
Di un gas reale, per esempio, si può esaminare il fattore di comprimibilità Z:
| Fig.18.1
Curve isoterme relative al fattore di comprimibilità Z per alcuni gas reali. Per il gas perfetto Z=1 (infatti, dalla legge generale del gas perfetto, il rapporto tra PV e nRT è eguale ad 1). Tutti i gas reali si comportano in modo anomalo, ma tendono all'ideale quando P tende a 0 e quando la loro T è alta. E' perciò necessario tener conto del volume delle molecole (detto covolume) e delle interazioni che esistono fra loro: occorre perciò fare delle correzioni della equazione di stato del gas perfetto o ideale. |
 |
Il modello strutturale dei gas reali tiene conto che, se si raffredda un gas reale a una T sufficientemente bassa, esso condensa (il gas ideale no), diventando liquido o solido; a T = 0 K il solido avrà un volume b: perciò il volume totale a disposizione del gas non è V, ma (V - b) in cui b è il volume molare del gas a 0 K.
Inoltre, nel gas reale, il moto delle particelle non è uniforme: esistono attrazioni e repulsioni, soprattutto quando le particelle sono vicine (prima e dopo un urto).
Ciò porta a una diminuzione della P rispetto all'ideale: Pideale = P + (a/V2)
in cui il termine a/V2 è chiamato P interna, o di coesione ed è un fattore legato alle forze di interazione intermolecolari.
L'equazione per i gas reali, detta di Van der Waals diventa perciò: (P + n2a/V2) (V-nb) = nRT
il fattore n dipende dal fatto che bisogna tenere conto del numero delle particelle (notare che n/V rappresenta la concentrazione).
A seconda che predomini l'effetto del volume (con effetto +DP) o quello delle forze di coesione (con effetto -DP) la P di un gas reale sarà maggiore o minore di quella del gas ideale.
Ad alta T gli effetti della coesione sono minori (poiché predomina l'energia cinetica delle particelle), mentre ad alta P il volume a disposizione per il moto diminuisce molto (parte di esso è infatti occupato dal covolume b delle particelle, che possiamo trascurare solo a bassa pressione).
gas reale |
a (dm6 atm mol-1) |
b (dm3 mol-1) |
He |
0,03412 | 0,02370 |
Ne |
0,217 | 0,02709 |
Ar |
1,345 | 0,03219 |
Kr |
2,318 | 0,03978 |
Xe |
4,194 | 0,05105 |
H2 |
0,2444 | 0,02661 |
O2 |
1,360 | 0,03183 |
N2 |
1,390 | 0,03913 |
Cl2 |
6,493 | 0,05632 |
HCl |
3,667 | 0,04081 |
CH4 |
2,253 | 0,04278 |
NH3 |
4,170 | 0,03707 |
CO |
1,485 | 0,03985 |
CO2 |
3,592 | 0,04267 |
Fig.18.2 Parametri di Van der Waals per alcuni gas reali. Si può notare che b (covolume) aumenta al crescere del numero atomico anche se non in modo drammatico (per Xe è poco più del doppio di He); per quanto riguarda invece a, che dipende dalle interazioni intermolecolari, le variazioni sono molto più evidenti (per Xe addirittura 120 volte che per He).
Nei calcoli per i gas reali usiamo, normalmente, la legge generale, poiché nelle condizioni ambientali normali risulta abbastanza attendibile (siamo abituati, nei calcoli stechiometrici, a fare notevoli approssimazioni).
Un valore che usiamo spesso è quello del volume molare del gas ideale a 0° C e 1 atm.
Ponendo così n = 1, T = 273; P = 1 atm; R = 0,082 dm3 atm mol-1 K-1, allora V = RT/P = 22.4 litri.
Nel trattare il comportamento del gas ideale e dei gas reali, abbiamo finora sempre considerato una sola specie chimica; ma se il sistema è costituito da una miscela di due o più gas che occupano lo stesso volume V, identificando ogni singola specie gassosa con i simboli A, B, ..i... e considerando che tutti si comportino come gas ideali, ognuno di essi seguirà la legge generale.
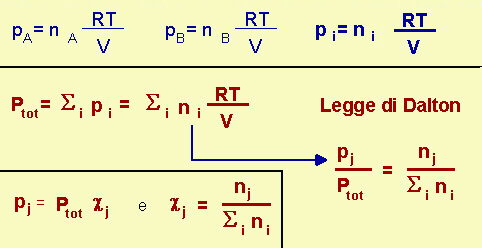
| Potremo
scrivere le relazioni in alto, in cui pi, detta pressione parziale del
gas i, è la pressione che il gas i eserciterebbe se occupasse da solo
tutto il volume disponibile, dato che, considerando gas ideali, le particelle sono
indistinguibili tra loro. Se dividiamo l'espressione relativa a un gas generico j per l'espressione relativa alla pressione totale Ptot, avremo la relazione a destra, dalla quale si ottiene poi quella in basso, in cui cj rappresenta la frazione molare del gas j. In conclusione, la pressione parziale di un gas j è data dal prodotto della sua frazione molare per la pressione totale. |
 |
I gas reali, come abbiamo visto, se sottoposti ad una adeguata pressione e portati ad una T abbastanza bassa, condensano, diventando prima liquidi, poi solidi.
Prendiamo in considerazione il passaggio alla fase liquida di un gas reale; portiamo in un diagramma P/V (diagramma di Andrews), i dati relativi e vediamo quali curve si ottengono, a seconda delle varie T.
| Fig.18.3
Diagramma di Andrews Le varie curve sono ottenute a diverse T: (T1, T2, TC, T3). Le isoterme a T > TC, come per esempio T3, hanno un andamento simile a quello dei gas ideali (ricordare che il gas ideale segue la legge di Boyle (PV)T = K, e corrisponde perciò, in questo schema, al ramo di un'iperbole equilatera).
Per isoterme con T < TC (T1, T2...) esiste il fenomeno della liquefazione del gas. Possiamo notare 3 parti distinte: nella curva T2, per esempio, un tratto (d-a), a bassa P, corrisponde alla legge di Boyle; una parte orizzontale in cui cala il volume ma la P resta costante (a-b) e infine una in cui la P cresce rapidamente a partire da b. |
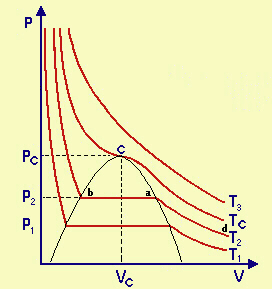 |
Supponiamo di comprimere il gas a T = T2 (partendo da d). In a inizia la liquefazione: da a a b diminuisce il volume, mentre P2 resta costante: questa P2 è quella esercitata dal gas in equilibrio con il liquido a T = T2 ed è detta tensione di vapore del liquido a quella temperatura. In b la liquefazione è totale: per forti aumenti di pressione, le DV sono molto piccole (in effetti i liquidi sono poco comprimibili).
A T = TC, l'isoterma ha un flesso, ma non si ha ancora liquefazione del gas.
Questa TC è chiamata temperatura critica del gas e sopra di essa non è possibile liquefare il gas, qualunque sia la P che si impone: il gas resta perciò sempre nel suo stato gassoso; sotto la campana la sostanza invece esiste come liquido e come vapore.
C è detto punto critico ed è identificato da una coppia di valori di P e di V:
PC= pressione critica
VC= volume critico
Questo tipo di comportamento è conseguenza necessaria della non idealità del gas; i parametri critici sono legati perciò alle costanti a e b dell'equazione di Van der Waals e si possono ricavare da essi.