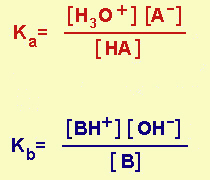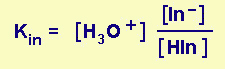Corso di chimica generale ed inorganica
Vai all'INDICE GENERALE
24 - acidi e basi
La prima
definizione di acido e di base è stata data dal chimico svedese Svante
Arrhenius
| Fig.24.1 Un ritratto
di Svante ArrheniusSvante August
Arrhenius (Uppsala 1859 - Stoccolma 1927), chimico e fisico svedese, contribuì a
porre le basi della chimica moderna. Compì gli studi superiori presso l'università di
Uppsala e ancora studente approfondì le proprietà di conducibilità elettrica delle
soluzioni elettrolitiche. Nel 1887 formulò la teoria della dissociazione elettrolitica,
in parte già esposta nella sua tesi di laurea, secondo cui nelle soluzioni elettrolitiche
i composti chimici presenti in soluzione si dissociano in ioni, anche quando non vi sia
corrente che attraversa la soluzione. Arrhenius postulò inoltre che il grado di
dissociazione aumenta quanto più viene diluita la soluzione, ipotesi che successivamente
si rivelò esatta solo per gli elettroliti deboli. La teoria di Arrhenius, inizialmente
ritenuta errata, fu poi accettata a livello generale, e divenne una delle pietre miliari
della chimica fisica e dell'elettrochimica moderne.
Nel 1889 egli osservò che la velocità delle
reazioni chimiche aumenta al crescere della temperatura con ritmo proporzionale alla
concentrazione delle molecole attivate. Nel 1895 Arrhenius divenne professore ordinario di
chimica all'università di Stoccolma e nel 1905 presidente dell'Istituto Nobel per la
chimica e la fisica. Tra i riconoscimenti dei quali fu insignito ricordiamo il premio
Nobel per la chimica, ottenuto nel 1903. Scrisse opere di chimica fisica, chimica
biologica, elettrochimica e astronomia.
(da Enciclopedia
Microsoft Encarta) |
 |
Il premio Nobel lo ottenne
proprio per la sua teoria sulla dissociazione elettrolitica. Egli disse che:
acido = molecola che,
dissociandosi, fornisce ioni H+
base = molecola che,
dissociandosi, fornisce ioni OH-
perciò, per un acido
HA ¨ H+ + A-
mentre per una base
BOH ¨ B+ + OH-
Ma la definizione non può andare bene
per sostanze come SO2, CO2, NH3, che pure rendono acida o
basica una loro soluzione acquosa, oltre a trascurare che, per esempio, NaOH non è
"una" molecola definita (ricordare i reticoli cristallini ionici).
Potremmo usarla in prima approssimazione,
definendo però acido una sostanza in grado di far aumentare
[H+] e analogamente per base una sostanza in
grado di far aumentare [OH-].
Usando questa nuova definizione
modificata, CO2 è acida perché, con l'acqua, reagisce:
CO2 + H2O
¨ HCO3-
+ H+
e NH3 basica:
NH3 + H2O
¨ NH4+
+ OH-
Più corretta e completa è la
definizione di J.N.Brønsted e di T.M.Lowry, del 1923,
che introduce il concetto di acido e base coniugati; così sarà:
acido = donatore di protoni
base = accettore di protoni
Si parla di "protoni" veri e
propri e la base non dipende dalla presenza del gruppo OH. Perciò saranno:
acidi: HCl,
HNO3, H2O,
NH4+, HS-,
Al(H2O)63+,
etc.
basi: H2O,
OH-, HS-, NH3,
Cl-, O2-, SO42-,
etc.
Le sostanze che possono comportarsi come
acidi e come basi, a seconda dell'ambiente in cui si trovano (H2O,
HS-, HSO4-, etc.)
sono dette anfiprotiche.
Si chiama base coniugata Bi
di un acido Ai quella che deriva da quell'acido e viceversa.
A1 |
+ |
B2 |
¨ |
A2 |
+ |
B1 |
H2O |
+ |
H2O |
¨ |
H3O+ |
+ |
OH- |
HCl |
+ |
H2O |
¨ |
H3O+ |
+ |
Cl- |
H2O |
+ |
NH3 |
¨ |
NH4+ |
+ |
OH- |
NH3 |
+ |
NH3 |
¨ |
NH4+ |
+ |
NH2- |
H2SO4 |
+ |
H2SO4 |
¨ |
H3SO4+ |
+ |
HSO4- |
Fig.24.2 Acidi e basi coniugate. Sono
indicati alcuni esempi.
Nella tabella, A1
e B1 sono coniugati, poiché l'acido A1
dà luogo alla base B1; analogamente sono coniugati B2
e A2.
Notare che, come l'acqua, anche NH3
e H2SO4 presentano
il fenomeno detto autoprotolisi (una molecola funge da acido, un'altra eguale da
base). Questo fenomeno è comprovato dal fatto, per esempio, che, come H2O,
anche NH3 liquida e H2SO4
puro permettono il passaggio di elettricità, cosa che non potrebbe avvenire se non
fossero presenti ioni nella soluzione.
| |
acido A1 |
base B1 |
|
acidità |
HClO4 |
ClO4- |
basicità |
massima |
HMnO4 |
MnO4- |
minima |
|
HClO3 |
ClO3- |
¯ |
|
H2SeO4 |
HSeO4- |
¯ |
|
HI |
I- |
¯ |
|
HBr |
Br- |
¯ |
|
HCl |
Cl- |
¯ |
|
HSO4- |
SO42- |
¯ |
|
HClO2 |
ClO2- |
¯ |
|
HNO2 |
NO2- |
¯ |
|
HF |
F- |
¯ |
|
CH3COOH |
CH3COO- |
¯ |
|
HClO |
ClO- |
¯ |
|
NH4+ |
NH3 |
¯ |
|
HCO3- |
CO32- |
¯ |
|
H2O2 |
HO2- |
¯ |
|
H2O |
OH- |
¯ |
acidità |
HS- |
S2- |
basicità |
minima |
OH- |
O2- |
massima |
Fig.24.3 Scala di acidità di una
serie di sostanze acide e di basicità delle basi coniugate corrispondenti. Quanto più è
forte l'acido, tanto più è debole la sua base coniugata e viceversa.
Gli acidi possono
essere distinti in idracidi, quando non
contengono ossigeno, come gli acidi alogenidrici: acido iodidrico HI,
acido bromidrico HBr, acido cloridrico HCl, acido
fluoridrico HF, oppure come l'acido solfidrico H2S
e l'acido azotidrico HN3; e in ossiacidi di formula
generale HnXOm.
Possiamo dedurre quale sia la forza di un
ossiacido in base a una regoletta matematica che prende in considerazione i coefficienti n
ed m della formula generale HnXOm.
m-n = 0 (HnXOn)
acidi debolissimi
(HClO, H3AsO3,
H4SiO4)
m-n = 1 (HnXOn+1)
acidi deboli e medi (HClO2,
H2CO3, H3AsO4)
m-n = 2 (HnXOn+2)
acidi forti
(HClO3, H2SO4,
H2SeO4)
m-n = 3 (HnXOn+3)
acidi fortissimi
(HClO4, HMnO4)
Non è possibile avere m-n = 4, perché
ciò comporterebbe un numero di ossidazione formale 9, incompatibile con la struttura
elettronica degli atomi.
Una ulteriore generalizzazione nella
definizione di acido è dovuta alla teoria di G.N.Lewis (1923), valida
anche per sistemi non acquosi.
acido = sostanza che può accettare
una coppia di elettroni
base = sostanza che può cedere
una coppia di elettroni non impegnati in legami chimici.
Così si possono giustificare tutte le
situazioni possibili:
acido |
+ |
base |
® |
|
H3O+ |
+ |
OH- |
® |
2 H2O |
BF3 |
+ |
NH3 |
® |
H3N®BF3 |
Ag+ |
+ |
2 CN- |
® |
Ag(CN)2- |
AlCl3 |
+ |
Cl- |
® |
AlCl4- |
Fig.24.4 Acidi e basi di Lewis.
Alcuni esempi di coppie acido-base di caratteristiche diverse.
Si tratta di una teoria molto generale,
ma spesso, dato che operiamo in ambiente acquoso, preferiamo usare quella di Brønsted-Lowry
per comodità.
Per essa, la forza di un acido
corrisponde alla sua tendenza a cedere un protone ad una base.
Alcuni acidi sono così forti
che, anche se in alte concentrazioni, la reazione di dissociazione è quasi totale,
quantitativamente spostata a destra
HA + H2O ¨ H3O+
+ A-
e perciò, se chiamiamo Ca
la concentrazione iniziale dell'acido, allora [H3O+]
= Ca
| Con acidi deboli, per
la reazione di dissociazione HA + H2O
¨ H3O+
+ A- si arriva ad
una situazione di equilibrio, con concentrazioni misurabili di HA, A-,
H3O+.
Quantitativamente la forza di un acido
è espressa dalla sua K di equilibrio di dissociazione,
in cui però la [H2O] è conglobata nella Ka
(dato che la sua attività o, in prima approssimazione, concentrazione, è costante)
Analogamente per le basi deboli
si ha
B + H2O ¨ BH+ + OH-
da cui è possibile ricavare la relativa Kb |
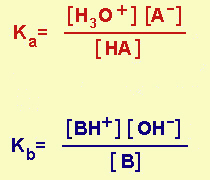 |
E' perciò possibile determinare il pH se si conosce la K.
Per acidi e basi molto forti la K
non viene data poiché è molto difficile da determinare (e comunque molto alta, ma poco
significativa).
Praticamente acidi e basi forti
sono elettroliti forti, cioè si dissociano completamente; acidi e basi deboli
sono elettroliti deboli, cioè si dissociano solo parzialmente.
I sali, che già allo stato solido
posseggono un reticolo ionico, sono elettroliti forti, e i loro ioni
(come tutti gli ioni), in acqua, vengono solvatati.
Alcuni di essi (Li+,
Na+, K+, Cl-,
NO3-, ClO4-,
I-, etc.) restano come tali anche dopo la solvatazione,
essendo acidi coniugati di basi molto forti o basi coniugate di acidi molto forti; perciò
non provocano nessuna variazione di pH.
Altri invece, dopo la solvatazione,
possono reagire con molecole di acqua di solvatazione secondo reazioni acido-base: avviene
il fenomeno della idrolisi (dal greco udro lusis = rottura dell'acqua), con conseguenze sul pH della soluzione.
Per esempio danno luogo a soluzioni con:
pH > 7
carbonato di sodio Na2CO3,
cianuro di potassio KCN, fluoruro di potassio KF, idrosolfuro di
sodio NaHS, acetato di sodio CH3COONa, etc.
pH < 7 nitrato
di ammonio NH4NO3,
cloruro di zinco ZnCl2, solfato
di alluminio Al2(SO4)3,
etc.
Si può capire ciò che succede, in base
alla teoria di Brønsted-Lowry; prendiamo come esempio il caso del cianuro di potassio:
KCN ® K+ + CN-
K+, solvatato, non
reagisce con H2O (è un acido debolissimo,
coniugato di una base forte), mentre CN- invece reagisce (è una base
forte, coniugata di un acido debole) secondo la reazione:
CN- + H2O ¨ HCN + OH-
ed essendoci un aumento di ossidrili, il pH
aumenta.
Analogamente, con nitrato d'ammonio:
NH4NO3 ® NH4+ + NO3-
NO3-,
solvatato, non reagisce con H2O (è una base
debolissima, coniugata di un acido forte), mentre NH4+
invece reagisce (è un acido forte, coniugato di una base debole):
NH4+ + H2O
¨ NH3
+ H3O+
ed essendoci un aumento di ioni idrogeno
solvatati, il pH diminuisce.
Chiamiamo costanti di idrolisi Ki
le costanti di equilibrio delle reazioni di idrolisi in cui [H2O]
è conglobata nella K.

Le Ki
si possono facilmente collegare con le Ka, le Kb,
la Kw.
In effetti il loro valore è,
normalmente, molto piccolo, cioè le moli di CN- e di NH4+
che reagiscono sono in percentuale molto bassa, ma sufficienti per provocare alte
variazioni di pH.
Se poi ambedue gli ioni dovuti alla
dissociazione elettrolitica del sale danno idrolisi (come succede, per esempio, con
acetato d'ammonio CH3COONH4,
o con carbonato di zinco ZnCO3) la variazione di pH
sarà minore e i calcoli più complessi.
Alcuni cationi
danno idrossidi che possono reagire sia come acidi sia come basi, a seconda dell'ambiente
e del pH della soluzione, e sono detti perciò anfoteri (per esempio Al3+,
Cr3+, Pb2+, Zn2+, etc.)
Al(OH)3 + H3O+
¨ Al(OH)2+
+ 2 H2O
Al(OH)3 + OH- ¨ Al(OH)4-
Abbiamo detto che anche piccole quantità
di ioni come NH4+, CN-,
possono provocare alte variazioni di pH.
Effetti ancora maggiori sul pH avvengono
ovviamente se mettiamo in soluzione acidi o basi molto forti.
Tale variazione può venire minimizzata
se, in soluzione, sono presenti un acido debole e un suo sale (HA e A-)
o una base debole e un suo sale (B e BH+). Queste sono dette soluzioni
tampone.
La loro importanza è enorme, in
particolare nei sistemi biologici: per esempio, il sangue umano ha pH @ 7,4 e non varia che di pochi centesimi di unità di pH, anche in
condizioni drammatiche; è infatti "tamponato"; se così non fosse, molte
reazioni biochimiche essenziali per la vita verrebbero modificate o rese impossibili, con
conseguenze irreparabili (l'acidosi del sangue è molto pericolosa).
Supponiamo di avere, in soluzione
acquosa, una concentrazione CA di un acido debole HA,
e una concentrazione CS di un suo sale A-.
Possiamo dire, approssimando, che
[HA] = CA (dato che l'acido è debole, perciò si dissocia
in minima parte, tanto più che è già presente A- che tende a far
regredire la già bassa dissociazione dell'acido) e che [A-] = CS
Sostituendo nella Ka
di equilibrio dell'acido questi valori, otteniamo
[H3O+] = Ka
CA/CS
Una eventuale diluizione (purché non
eccessiva) non porta a variazioni di pH, in quanto il rapporto CA/CS
non cambia.
Se vengono aggiunte alla soluzione
quantità di acido o di base, relativamente piccole rispetto alla quantità del tampone,
queste danno reazione quantitativa con A- o con HA; il rapporto CA/CS
cambia, ma di poco, perciò cambia poco anche il pH.
I calcoli sono più semplici se si passa
ai logaritmi
pH = pKa + lg CS/CA
L'effetto sul pH viene così
"tamponato".
E' chiaro che il sistema sarà in grado
di "tamponare" quantità tanto maggiori di acido o di base, quanto maggiori sono
CA e CS (non il loro
rapporto!). Si parla, in questa ottica, di potere tamponante.
Un comportamento analogo presentano
sostanze dette indicatori acido-base, che hanno colori diversi se sono in forma
indissociata o dissociata.
Gli indicatori sono acidi o basi deboli
e, poiché ne basta una concentrazione bassissima per evidenziare il viraggio (variazione
di colore), non influenzano il pH della soluzione durante la titolazione
(procedimento di determinazione, nel nostro caso, della quantità di acido o di base in
una soluzione mediante aggiunta di soluzioni note di base o di acido).
Se chiamiamo H In un
indicatore generico:
H In + H2O ¨ H3O+
+ In-
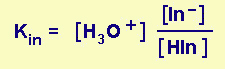
Il rapporto [HIn] / [In-]
viene molto influenzato dal pH: praticamente la soluzione assumerà il colore di HIn
quando il rapporto è >10; il colore di In- quando il rapporto
è <0,1.
Gli indicatori sono perciò molto utili nelle
titolazioni acido-base.